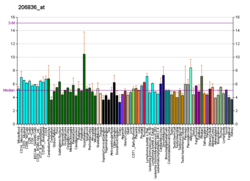
SLC6A3
SLC6A3 (ингл. ) — аксымы, шул ук исемдәге ген тарафыннан кодлана торган югары молекуляр органик матдә.[29][30]
Искәрмәләр[үзгәртү | вики-текстны үзгәртү]
- ↑ 1,0 1,1 UniProt
- ↑ 2,00 2,01 2,02 2,03 2,04 2,05 2,06 2,07 2,08 2,09 2,10 2,11 2,12 2,13 2,14 2,15 2,16 2,17 2,18 2,19 2,20 2,21 2,22 2,23 2,24 2,25 2,26 2,27 2,28 2,29 2,30 2,31 2,32 2,33 2,34 2,35 2,36 2,37 2,38 2,39 2,40 2,41 2,42 2,43 2,44 2,45 2,46 2,47 GOA
- ↑ 3,00 3,01 3,02 3,03 3,04 3,05 3,06 3,07 3,08 3,09 3,10 3,11 3,12 3,13 GOA
- ↑ Caron M. G. Functional interaction between monoamine plasma membrane transporters and the synaptic PDZ domain-containing protein PICK1 // Neuron / K. Brose — Cell Press, Elsevier BV, 2001. — ISSN 0896-6273; 1097-4199 — doi:10.1016/S0896-6273(01)00267-7 — PMID:11343649
- ↑ 5,0 5,1 5,2 Caron M. G. Effect of torsinA on membrane proteins reveals a loss of function and a dominant-negative phenotype of the dystonia-associated DeltaE-torsinA mutant // Proc. Natl. Acad. Sci. U.S.A. / M. R. Berenbaum — [Washington, etc.], USA: National Academy of Sciences [etc.], 2004. — ISSN 0027-8424; 1091-6490 — doi:10.1073/PNAS.0308088101 — PMID:15505207
- ↑ 6,0 6,1 6,2 Wersinger C., Prou D., Vernier P. et al. Modulation of dopamine transporter function by alpha-synuclein is altered by impairment of cell adhesion and by induction of oxidative stress // FASEB J. — FASEB, 2003. — ISSN 0892-6638; 1530-6860 — doi:10.1096/FJ.03-0152FJE — PMID:12958153
- ↑ 7,0 7,1 Jiang W., Prokopenko O., Wong L. et al. IRIP, a new ischemia/reperfusion-inducible protein that participates in the regulation of transporter activity // Mol. Cell. Biol. — ASM, 2005. — ISSN 0270-7306; 1098-5549; 1067-8824 — doi:10.1128/MCB.25.15.6496-6508.2005 — PMID:16024787
- ↑ 8,0 8,1 8,2 8,3 Livstone M. S., Thomas P. D., Lewis S. E. et al. Phylogenetic-based propagation of functional annotations within the Gene Ontology consortium // Brief. Bioinform. — OUP, 2011. — ISSN 1467-5463; 1477-4054 — doi:10.1093/BIB/BBR042 — PMID:21873635
- ↑ C Saunders, Ferrer J. V., L Shi et al. Amphetamine-induced loss of human dopamine transporter activity: an internalization-dependent and cocaine-sensitive mechanism // Proc. Natl. Acad. Sci. U.S.A. / M. R. Berenbaum — [Washington, etc.], USA: National Academy of Sciences [etc.], 2000. — ISSN 0027-8424; 1091-6490 — doi:10.1073/PNAS.110035297 — PMID:10823899
- ↑ Giros B., Jaber M., Jones S. R. et al. Hyperlocomotion and indifference to cocaine and amphetamine in mice lacking the dopamine transporter // Nature / M. Skipper — NPG, Springer Science+Business Media, 1996. — ISSN 1476-4687; 0028-0836 — doi:10.1038/379606A0 — PMID:8628395
- ↑ Matthies H. J., Robertson S. D., Javitch J. Flotillin-1 is essential for PKC-triggered endocytosis and membrane microdomain localization of DAT // Nat. Neurosci. — NPG, 2011. — ISSN 1097-6256; 1546-1726 — doi:10.1038/NN.2781 — PMID:21399631
- ↑ Wersinger C., Prou D., Vernier P. et al. Modulation of dopamine transporter function by alpha-synuclein is altered by impairment of cell adhesion and by induction of oxidative stress // FASEB J. — FASEB, 2003. — ISSN 0892-6638; 1530-6860 — doi:10.1096/FJ.03-0152FJE — PMID:12958153
- ↑ 13,0 13,1 Matthies H. J., Robertson S. D., Javitch J. Flotillin-1 is essential for PKC-triggered endocytosis and membrane microdomain localization of DAT // Nat. Neurosci. — NPG, 2011. — ISSN 1097-6256; 1546-1726 — doi:10.1038/NN.2781 — PMID:21399631
- ↑ 14,0 14,1 14,2 Navaroli D. M., Stevens Z. H., Uzelac Z. et al. The plasma membrane-associated GTPase Rin interacts with the dopamine transporter and is required for protein kinase C-regulated dopamine transporter trafficking // J. Neurosci. / M. Picciotto — Society for Neuroscience, 2011. — ISSN 0270-6474; 1529-2401 — doi:10.1523/JNEUROSCI.2649-11.2011 — PMID:21957239
- ↑ Navaroli D. M., Stevens Z. H., Uzelac Z. et al. The plasma membrane-associated GTPase Rin interacts with the dopamine transporter and is required for protein kinase C-regulated dopamine transporter trafficking // J. Neurosci. / M. Picciotto — Society for Neuroscience, 2011. — ISSN 0270-6474; 1529-2401 — doi:10.1523/JNEUROSCI.2649-11.2011 — PMID:21957239
- ↑ 16,00 16,01 16,02 16,03 16,04 16,05 16,06 16,07 16,08 16,09 16,10 16,11 16,12 16,13 16,14 IUPHAR/BPS Guide to PHARMACOLOGY
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ Open Targets Platform
- ↑ HUGO Gene Nomenclature Commitee, HGNC:29223 (ингл.). әлеге чыганактан 2015-10-25 архивланды. 18 сентябрь, 2017 тикшерелгән.
- ↑ UniProt, Q9ULJ7 (ингл.). 18 сентябрь, 2017 тикшерелгән.
Чыганаклар[үзгәртү | вики-текстны үзгәртү]
- Степанов В.М. (2005). Молекулярная биология. Структура и функция белков. Москва: Наука. ISBN 5-211-04971-3.(рус.)
- Bruce Alberts, Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts, Peter Walter (2002). Molecular Biology of the Cell (вид. 4th). Garland. ISBN 0815332181.(ингл.)
| Бу — аксым турында мәкалә төпчеге. Сез мәкаләне үзгәртеп һәм мәгълүмат өстәп, |